I funghi (Fungi, L. 1753, dal latino) o miceti (dal greco μύκης) sono un regno di organismi eucarioti, unicellulari e pluricellulari a cui appartengono anche i lieviti e le muffe. Il regno comprende più di 100.000 specie conosciute, benché la diversità sia stata stimata in più di 3 milioni di specie.
Classificati scientificamente da Linneo come Piante, i funghi sono stati poi elevati al rango di regno da Nees nel 1817 e da Whittaker nel 1968. Altri organismi storicamente classificati come funghi sono tuttora di classificazione incerta: Thomas Cavalier-Smith ha proposto un sesto regno, Chromista, comprendente le classi dei Hyphochytridiomycetes e Oomycetes. I moderni studi molecolari hanno contribuito a produrre un ordinamento sistematico più obiettivo, basato sulla filogenesi, che promette un maggior grado di stabilità.
La disciplina che studia i funghi si chiama micologia.
Caratteristiche
Gli organismi del regno dei funghi sono accomunati dalle seguenti caratteristiche:
- alimentazione eterotrofa: i funghi si nutrono di sostanze organiche elaborate da altri organismi;
- mancanza di tessuti differenziati e di elementi conduttori di linfa;
- sistema riproduttivo tramite spore, e non attraverso uno stadio embrionale come animali e piante.
Al regno dei funghi appartengono inoltre organismi eterotrofi riproducentisi da spore, da molto semplici (unicellulari) a più complessi (pluricellulari) con struttura vegetativa eventualmente organizzata in cellule formanti strutture filamentose dette ife o micelio primario, non differenziate in tessuti. A differenza delle cellule vegetali, che hanno una parete costituita prevalentemente da cellulosa, la parete cellulare dei funghi è costituita da differenti glucani (ß-glucani prevalentemente non cellulosici) e da un altro polisaccaride, la chitina, polimero dell'aminozucchero N-acetil-glucosamina, presente anche nell'esoscheletro degli artropodi. La chitina, rispetto alla cellulosa è molto più resistente alla degradazione microbica. In passato i polisaccaridi strutturali chitinosi venivano chiamati micosina.
Riguardo ai polisaccaridi di riserva, i funghi possono accumulare, analogamente agli animali, sostanze di riserva energetica sotto forma di glicogeno, differentemente dai vegetali che utilizzano l'amido. Le cellule che costituiscono le ife possono essere mono o polinucleate e possono essere divise da setti. La presenza o meno dei setti è una caratteristica distintiva di alcuni gruppi di funghi rispetto ad altri. Negli Zigomiceti, infatti, le ife non sono settate, cosa che invece è presente negli Ascomiceti, nei Basidiomiceti e nei Deuteromiceti.
Il setto può essere:
- intero, senza poro;
- perforato, con poro centrale che consente il passaggio del protoplasma e di organi cellulari:
- a barile o doliporo, con poro circondato da un bordo costituito da fibre di chitina che arriva a formare una struttura cilindrica (presente in alcuni gruppi di Basidiomiceti).
Le ife si sviluppano all'interno del substrato di crescita fino a formare un reticolo intrecciato detto micelio.
Una delle caratteristiche di alcuni funghi è quella di emettere luce, come ad esempio la clitocibe dell'ulivo (Omphalotus olearius), che si illumina per via delle lamelle bioluminescenti.
Riproduzione
I funghi si possono riprodurre in maniera asessuata o in maniera sessuata attraverso la produzione di spore dette endospore, come avviene per la maggior parte di essi. Le spore possono essere prodotte in maniera sessuata, attraverso la fusione di due o più nuclei, o asessuata, senza che ciò avvenga. A seconda del phylum cui appartengono i funghi che le producono si parlerà di ascospore (Ascomycota), basidiospore (Basidiomycota) o zigospore (Zygomycota).
Riproduzione asessuata
La riproduzione asessuata può avvenire per:
- Scissione binaria
- Come avviene nei lieviti (Ascomycota), consiste nella divisione della cellula madre in due cellule figlie uguali, con lo stesso patrimonio genetico attraverso un processo chiamato mitosi. I funghi che adottano questo sistema riproduttivo hanno un accrescimento esponenziale.
- Gemmazione
- Comune anch'essa nei lieviti, è un sistema in cui le cellule figlie compaiono come protuberanze (gemme) della cellula madre dalla quale poi si possono distaccare diventando autonome o possono restare attaccate formando una colonia; è diversa dalla scissione in quanto nella gemmazione avviene una ripartizione diseguale del citoplasma.
- Frammentazione
- Avviene con il distacco di una parte più o meno sviluppata che si accresce in maniera indipendente.
- Sporogenesi
- Attraverso un processo mitotico vengono prodotte spore (mitospore), capaci di generare un nuovo individuo, in cellule specializzate (sporocisti). Le mitospore, protette da una spessa parete, possono essere mobili e flagellate (zoospore), oppure no (aplanospore). In alcuni gruppi di funghi viene prodotto un particolare tipo di aplanospore, esternamente alla sporocisti, chiamate conidiospore.
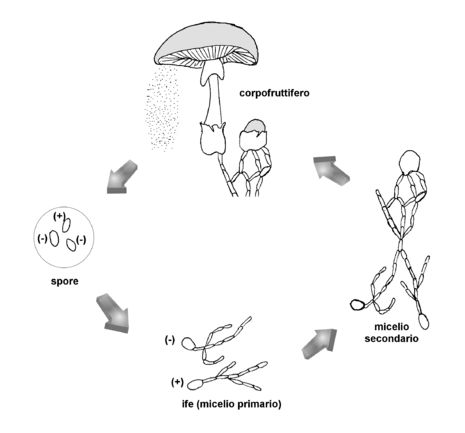
Riproduzione sessuata
La riproduzione sessuata è subordinata alla produzione di spore che, prodotte a milioni da ciascun individuo, vengono diffuse sostanzialmente attraverso il vento, l'acqua o gli insetti. In numerose specie appartenenti ad esempio ai phyla Oomycota, Zygomycota ed Ascomycota le spore maschili e femminili si uniscono formando un'unica struttura polinucleata che in seguito alla fusione dei nuclei (evento che non avviene subito dopo la fusione tra le spore) subisce meiosi producendo spore aploidi, le quali non appena trovate le condizioni adatte germinano formando nuovi miceli. Nelle specie appartenenti al phylum dei Basidiomycota la spora di una determinata polarità sessuale, una volta raggiunto il terreno o il substrato più adatto, nelle condizioni più favorevoli di umidità e temperatura, germina formando un filamento di cellule detto ifa (micelio primario). Per poter completare il ciclo biologico e organizzare le strutture riproduttive, dal micelio primario si deve passare al micelio secondario, vero organismo fungino. Così l'ifa generata da una spora con carica maschile si unisce ad una con carica sessuale opposta, fenomeno noto come somatogamia, per formare il micelio secondario che genererà il frutto (carpoforo) portatore di nuove spore.
Quando in un micelio i nuclei cellulari, nell'ambito dello stesso citoplasma, hanno un patrimonio genetico simile si parla di omocariosi. Può avvenire, invece, che nello stesso citoplasma siano presenti nuclei geneticamente differenti a seguito di mutazione o di fusione di ife geneticamente diverse, in tal caso si parla di eterocariosi, fenomeno scoperto dal micologo tedesco Buryef nel 1912. L'eterocariosi è fondamentale per l'evoluzione dei funghi in quanto garantisce l'opportuno mescolamento del patrimonio genetico con una conseguente maggior variabilità delle specie.
Nutrizione
Tutti i funghi sono eterotrofi, cioè ricavano le sostanze nutritive dall'ambiente esterno, assorbendole attraverso le pareti. I funghi costituiscono un anello importante negli ecosistemi in quanto facilitano la decomposizione del materiale organico, permettendo così la chiusura del ciclo della materia – rendendola nuovamente bio-disponibile.
L'eterotrofia dei funghi li costringe a un tipo di vita dipendente che si può differenziare in tre modalità, distinte in base ai rapporti del fungo stesso con il substrato di crescita: saprofitismo, parassitismo e mutualismo.
A seconda delle loro esigenze nutritive i funghi si dividono in saprofiti, parassiti e simbionti o mutualistici.

Saprofiti
Si definiscono saprofiti tutti quei funghi che degradano sostanze non viventi di origine animale o vegetale in composti meno complessi. Ad esempio vari composti organici come la lignina e la cellulosa vengono aggredite e disgregate da una miriade di differenti funghi, che con i loro enzimi sono in grado di smontarli e nutrirsene in una catena metabolica molto intricata rendendo questi composti sempre più semplici fino a ottenere un residuo minerale assimilabile dal fungo. Ogni fungo occupa una propria posizione in questa catena di demolitori altamente specializzati, tanto che se per una qualsiasi ragione un anello in questa successione venisse a mancare il processo metabolico si interromperebbe e l'insieme di organismi dipendenti dai precedenti muore. In pratica non esiste composto organico che i funghi non riescano a degradare. Ad esempio, la specie Hermodendron resinae è capace di metabolizzare il cherosene. Si comprende il ruolo di estrema importanza che questi organismi hanno nel riciclare la materia organica di rifiuto.
Parassiti
Si definiscono parassiti quei funghi che si nutrono di organismi viventi, portandoli a volte gradatamente a morte. In natura essi operano la selezione dei più forti. Alcuni fra questi funghi, come ad esempio Armillaria mellea, dopo un iniziale comportamento da simbionte, diventano parassiti, per cui l'ospite (una pianta) viene ucciso, continuano poi con comportamento saprofita a nutrirsi della loro vittima anche quando questa è ormai morta; al contrario quelli definiti parassiti obbligati per distinguerli dai precedenti che vengono detti facoltativi, muoiono se muore il loro ospite. Il parassitismo colpisce anche gli animali, l'uomo, gli insetti e gli stessi funghi, con specializzazioni ancora una volta anche estreme, ad esempio esistono funghi specializzati nel degradare solo le tegmine delle cavallette oppure di colpire una particolare specie di insetto. Ne esistono anche di predatori, capaci cioè di catturare, con trappole anche sofisticate (cappi strozzanti, bottoni adesivi), le loro prede. Di recente, si tenta con successo di utilizzare questi parassiti nella lotta biologica contro specie che sono risultate resistenti agli insetticidi. Ad esempio, le zanzare del genere Anopheles portatrici della malaria, vengono uccise da Beauveria bassiana; basta infatti spruzzare una emulsione di acqua, olio e micelio, dove l'olio serve a conservare l'umidità necessaria perché il fungo sopravviva.

grilli infettati
Simbionti
Si definiscono simbionti quelle forme di parassitismo controllato in cui una specie si avvantaggia dell'ospite e questi trae vantaggio dalla contaminazione col “parassita“; lo scambio è alla fine mutualistico. Ad esempio il fungo estrae zuccheri dalle radici della pianta ma per scambio chimico cede sali minerali, azoto, potassio, fosforo. Il processo di infezione viene detto micorriza. Il fungo cede anche acqua, nel costruire le proteine durante il processo di polimerizzazione tra il gruppo amminico di un amminoacido e il gruppo carbossilico di un secondo, di cui la pianta attraverso l'assorbimento radicale si impadronisce. Si comprende come in caso di siccità questo meccanismo possa essere di grande aiuto. In un altro caso di simbiosi (Orchidee), il fungo cede zuccheri alla piantina in crescita, almeno fintanto che non si sviluppa il processo di fotosintesi. Poiché il seme della pianta è estremamente piccolo e non contiene praticamente carboidrati, la simbiosi è qui vitale. I funghi possono anche formare simbiosi con delle alghe per formare i licheni. Questi organismi pionieri sono formati da un fungo (micobionte) e da un'alga verde (fotobionte) e talvolta cianobatteri (o alghe azzurre).
Funghi patogeni
causa di tigna in cani e umani
Molte specie di funghi possono causare patologie all'uomo, agli animali e alle piante. Per l'uomo e gli animali sono patogeni alcuni funghi microscopici, che sono causa di micosi, come le tigne e il piede d'atleta. Tra gli agenti alcuni funghi dei generi Trichophyton e Microsporum.
Le piante sono attaccate da parecchi funghi, che causano diverse patologie: marciumi alle radici, come i funghi del genere Armillaria o Rosellinia; marciumi al colletto, come quelli causati da Phytophthora o Pythium; presenza di muffe sulle foglie, come nel caso dell'oidio della vite; marciumi sui frutti, come i funghi del genere Monilinia; disseccamenti dei rami, come i funghi del genere Fusarium o Verticillium. La peronospora è sicuramente un patogeno ma non è più ormai classificata nel regno dei Fungi.
Funghi tossici
{da: dott. Claudio Angelini, in: AMINT: «Tutto Funghi», ed. Giunti
Le intossicazioni da funghi, chiamate più propriamente micetismi, sono causate da quei funghi che contengono sempre, già allo stato fresco, concentrazioni più o meno elevate di sostanze tossiche per l'uomo.
False intossicazioni
Pur rappresentando in ltalia la maggior parte delie intossicazioni legate al consumo dei funghi (quasi il 66%) in realtà non sono dovute al consumo di funghi velenosi ma di funghi appartenenti a specie di per sè commestibili, divenute tossiche in determinate situazioni, determinando quadri clinici specifici, rientrano tutte in una generica sindrome gastroenterica, che può essere quindi espressione sla di "vera" che di "falsa" intossicazione da funghi.
Sindromi a lunga latenza
I sintomi compaiono da sei ore a uno o più giorni dal pasto. Potenzialmente gravi o mortali. La gravità è dovuta a una lunga latenza che non consente una immediata terapia finalizzata alla eliminazione dal tubo gastro enterico delle sostanze tossiche ingerite.
Sindrome falloidea
Tossine responsabili sono amatossine, fallotossine, virotossine. La dose letale di amatossine è 6-7 mg (0,1 mg per Kg di peso corporeo) contenuti in c.a. 50 g di fungo fresco. Sono specie responsabili Amanita phalloides e altre dello stesso gruppo, alcune Lepiota di piccola taglia. La tossina è presente anche in alcune specie dei generi Galerina, Gonocybe e Proliotina. Il quadro clinico è costituito da 3 fasi:
- periodo di latenza. I disturbi compaiono da 6 a 24 ore dopo l"íngestione, in media da 10 a 12 ore.
- fase gastrointestinale (coleriforme}. Dolori addominali, sudorazione,vomito incoercibile e diarrea profusa
- fase epatica. insufficienza epatica grave
Sindrome orellanica
L'orellanina è una micotossina citotossica contenuta nelle specie di funghi Cortinarius orellanus e Cortinarius rubellus responsabile della sindrome orellanica. Fu isolata per la prima volta nel 1955 dal medico polacco Stanisław Grzymała ma la struttura chimica è rimasto sconosciuta fino all'ultima metà degli anni settanta quando i chimici polacchi Antkowiak e Gessner hanno scoperto che l'orellanina appartiene ad un gruppo di composti chiamati bipiridine, una doppia struttura ad anello in cui entrambi gli anelli sono piridine (anelli eterociclici con un atomo di azoto). Antkowiak e Gessner scoprirono anche una sostanza simile, l'orellina che pur essendo affine dal punto di vista strutturale non è tossica. Chimicamente si tratta di una bipiridina N-ossido. Nella forma più stabile dell'orellanina gli atomi di azoto sono carichi positivamente, cosa che non avviene nell'orellina che, nella sua forma stabile è neutra. L'orellanina, che possiede una struttura bipiridinica, provoca gravi lesioni e necrosi renali. Le bipiridine con atomi di azoto caricati positivamente sono già note per la loro velenosità. Il principale meccanismo di tali composti è che essi disturbano importanti reazioni redox nell'organismo catturando uno o due elettroni da altre molecole generando altre reazioni redox indesiderate. I prodotti finali di tali reazioni possono essere ioni perossidi o superossidi, dannosi per le cellule. Con buona probabilità l'orellanina agisce in questo modo, anche se non è stato ancora ben individuato il modo con cui disturba le reazioni redox causando gravi danni renali. A 150 °C l'orellanina si decompone lentamente in orellina e ossigeno. Alla temperatura di 267 °C la decomposizione avviene in maniera esplosiva. Non è solubile in solventi organici e in acqua.
- periodo di latenza. I disturbi compaiono da 3-4 giorni fino a 20 gg. dopo l"ïngestione.
- I fase: dopo 4-9 ore compaiono secchezza della mucosa orale, sete insaziabile, urinamento continuo; quindi si passa a una seconda fase con mancanza di urina, vomito, diarrea, dolori addominali; infine la sindrome gastrointestinale regredisce rapidamente finché il soggetto va incontro ad un periodo di benessere (remissione)
- II fase: alla I fase segue la fase di insufficienza renale acuta (IRA), l'intossicazione non ben trattata provoca la morte per uremia.
Sindrome giromitrica
La sindrome giromitriana o sindrome giromitrica trattasi di una sindrome dovuta alla ingestione di funghi primariamente del genere Gyromitra, o Cudonia, (soprattutto ma non solo Gyromitra esculenta), la sindrome si manifesta dopo alcune ore dalla ingestione, i primi sintomi si hanno dalle 6 alle 24 ore dopo aver ingerito funghi tossici. Terapie a base di epatoprotettori, acido folico e vitamina B6 di norma portano alla guarigione. La dose letale per l'uomo è di 30–50 mg/kg. La sintomatologia dovuta all'attività delle tossine del fungo, tra le quali la gyromitrina, un composto idrazinico, esordisce con cefalea, vertigini, pesantezza epigastrica, emesi incoercibile, diarrea. Ai sintomi gastrointestinali seguono sintomi a carico del sistema nervoso centrale, quali sonnolenza o agitazione, convulsioni, coma e disidratazione, dispnea. Nei casi mortali nefrite interstiziale, collasso cardiocircolatorio e coma per insufficienza acuta epatorenale con ittero. L'attività della giromitrina consiste nel portare a deplezione di vitamina B6, piridossina, impedendo la sintesi del neurotrasmettitore GABA. A livello epatico, invece, la giromitrina conduce a deplezione dei citocromi P450 dei microsomi.
Specie di funghi che la determinano:
- Cudonia circinans
- Gyromitra esculenta
- Gyromitra gigas
- Gyromitra infula
Specie di funghi sospetti di determinarla:
- Helvella crispa
- Helvella elastica
- Helvella lacunosa
- Leotia lubrica
Il principio attivo è la gyromitrina così chiamato perché estratto dall'ascomicete dove è presente in maggiore quantità. Sostanzialmente la gyromitrina è composta da un mix di idrazine fra cui N-metil, N-formil.
Sindrome acromelagica
L’eritromelalgia o malattia di Mitchel è una manifestazione patologica dovuta a vasodilatazione parossistica, aumento della temperatura corporea, arrossamento dei piedi e delle mani. (da WIKIPEDIA). La malattia è stata descritta per la prima volta nel 1834, ma solo nel 1878 il medico statunitense Silas Weir Mitchell coniò il termine eritromelalgia. La sindrome è caratterizzata da un aumento della temperatura cutanea, vasodilatazione parossistica, in misura predominante agli arti inferiori, dolore urente alle estremità corporee, eritema, rossore. La posizione declive della parte interessata, il semplice contatto con le lenzuola, e l’esercizio fisico aggravano la manifestazione patologica. I dolori possono essere lievi e localizzati, oppure diffusi; essi sono esacerbati dalla esposizione al calore, e vengono attenuati dal freddo. La correlazione con alcune specie fungine è stata descritta inizialmente in Giappone nel 1987 (Nakamura., 1987). Nel 1996, nella Savoia francese vi fu una intossicazione collettiva, nella quale rimasero coinvolte 5 persone per aver confuso la Paralepista flaccida (Sowerby) Vizzini = Lepista inversa (Scop.) Pat. con la Paralepistopsis amoenolens (Malençon) Vizzini = Clitocybe amoenolens Malençon, I soggetti intossicati presentavano a distanza di 24 ore una sintomatologia dolorosa alle estremità dei piedi e delle mani. Nel 2001 (Saviuc et al., 2001) descrissero per la prima volta un quadro clinico definito di eritromelalgia, riconducibile alla specie Paralepistopsis amoenolens. Nel 2002 si è avuto un caso di intossicazione collettiva in Abruzzo, nel quale rimasero coinvolte sette persone (Leonardi et al., 2002) riconducibile sempre alla stessa specie fungina; altri casi sono stati segnalati sempre in Abruzzo da (Marinetti & Recchia, 2005). Specie responsabili in Occidente: la Paralepistopsis amoenolens (Malençon) Vizzini, 2012 (= Clitocybe amoenolens Malençon); in Oriente: la Paralepistopsis acromelalga (Ichimura) Vizzini, (= Clitocybe acromelalga Ichimura). Possibili confusioni per i raccoglitori ci sono tra: Paralepistopsis amoenolens (Malençon) = Clitocybe amoenolens Malençon e Paralepista flaccida (Sowerby) Vizzini = Lepista inversa (Scop.) Pat. Altre possibili confusioni si hanno con la Paralepista flaccida (Sowerby) Vizzini = Lepista flaccida (Sowerby) Pat.
Tossine
Dalla Paralepistopsis acromelalga (Ichimura) Vizzini, sono stati estratti degli acidi acromelici (A-E) acido N-(gamma-aminobutyryl)-L-glutammico (Konno et al., 1988) (Assisi F. et al., 2010). Anche da Paralepistopsis amoenolens (Malençon) Vizzini, sono state estratti gli stessi acidi acromelici (Bessard et al., 2004) attraverso un sistema combinato di spettrometria di massa e cromatografia liquida (Assisi F. et al., 2010). Gli acidi acromelici risultano essere implicati nella sindrome acromelalgica. Strutturalmente sono simili all’acido kainico e domoico, i quali agiscono come neuromediatori eccitatori fisiologici e pertanto responsabili dello stato iperemico e delle reazioni di tipo infiammatorio che si verificano alle estremità corporee (Assisi F. et al., 2010).
Meccanismo d'azione
Gli acidi acromelici, avendo una struttura simile all’acido kainico e domoico, agirebbero sui recettori periferici del glutammato (Follesa P. et al., 2009) i quali sono presenti sulle fibre amieliniche sensitive cutanee. Il quadro è essenzialmente di tipo periferico e pertanto questo fatto giustifica le sintomatologie dolorose tipiche dell’eritromelalgia. Inoltre gli acidi acromelici non oltrepasserebbero la barriera ematoencefalica e quindi la loro azione si esplica soltanto sulle terminazioni nervose cutanee. A livello istopatologico si è evidenziato un edema cutaneo senza infiammazione dei vasi sanguigni ed una infiltrazione mononucleare perivascolare (Diaz 2005) (Assisi F. et al., 2010). Sottoponendo i ratti ad una sindrome acromelalgica di tipo sperimentale, si è osservata in loro: ipotonia muscolare, alterazioni motorie, eritema alle zampe, degenerazioni neuronali sul nervo sciatico, perdite di peso, lesioni cutanee (Assisi F. et al., 2010) (Follesa P. et al., 2009).
Sintomatologie cliniche
L’incubazione è di 24-72 ore, a volte la manifestazione clinica si osserva anche in sesta giornata, dopo l’ingerimento della specie fungina responsabile. Si hanno: parestesie, edemi alle estremità colpite, iperemia cutanea, dolori parossistici notturni di tipo urente alle estremità degli arti inferiori e delle mani, vasodilatazione, insonnia, astenia. Le manifestazioni si protraggono per 8 giorni, fino ad arrivare a 3-5 settimane (Assisi F. et al., 2010). Il recupero può aversi anche dopo 2-4 mesi. In questa sindrome vi è l’assenza dei sintomi precoci riferibili all’apparato gastroenterico. Si nota altresì l’assenza delle alterazioni dei parametri bioumorali (referti di laboratorio). La sintomatologia dolorosa può interessare la gola, il naso, i padiglioni auricolari. Pasti abbondanti e ripetuti nel tempo, aggravano la sintomatologia clinica. (Follesa P. et al., 2009).
Terapie
Si consiglia il riposo a letto ed il sollevamento degli arti inferiori, evitando la deambulazione, poiché ogni movimento accentua le manifestazioni dolorose. Un rimedio efficace è il freddo. E’ scarsa la risposta degli antinfiammatori e dei dolorifici. L’acido acetilsalicilico (650 mg 1-4 volte/die) può produrre una rapida e prolungata remissione della sintomatologia. I farmaci che agiscono come vasodilatatori vanno evitati, i vasocostrittori possono dare effetti benefici. Non essendoci sintomi precoci, l’uso del carbone vegetale è inefficace (Assisi F. et al., 2010).
(Testo da: https://www.micologiaprofessionale.it/sindrome-acromelalgica-o-eritromelalgica/)
Sindrome rabdomiolitica
Principale specie responsabile di questo tipo di intossicazione è il Tricholoma equestre, fino a poco tempo fa ritenuto commestibile, talmente ricercato che era stato inserito nelle classifiche nazionali di vendita. Poi, verso l'inizio degli anni 2000, una rivista scientifica riportò che in Francia si erano verificati casi di avvelenamento da funghi di questo tipo, portando i soggetti alla stessa conclusione sintomatologica. Alla fine, venne accertato specie responsabile il T. equestre; non è stata isolata con sicurezza una micotossina capace di indurre specificatamente questo tipo di lesioni a carico del tessuto muscolare.
Una delle principali sindromi indotte da questo tipo di avvelenamento è la rabdomiolisi, una sindrome caratterizzata da una distruzione diffusa delle cellule muscolari con conseguente ipertermia, ipotermia, ischemia, disturbi metabolici ecc. A livello sintomatico, il soggetto si sente improvvisamente stanco, debole e accusa dolori muscolari accompagnati da crampi. Segue poi una fase di malessere generale, sudorazione, malfunzionamento dell'attività renale con emissione di urine di colore scuro. Le Autorità sanitarie italiane hanno vietato, con Decreto ministriale dell'agosto 2002, la raccolta e il commercio del T. equestre.
Sindrome di Szechwan
In seguito ad alcune intossicazioni verificatesi tra il 1970 ed il 1980 in America, presso ristoranti cinesi, l’ematologo D. E. Hammerschmidt mise in relazione nel 1980, questa intossicazione con il consumo del fungo Auricularia nigricans (Fr.) Birkebak, Looney & Sánchez-García, in Looney, Birkebak & Matheny, N. Amer. Fung. 8(6): 12 (2013). Sinonimi: Auricularia polytricha (Mont.) Sacc., (1885) = Hirneola polytricha (Mont.) Fr., (1849). La sintomatologia dette origine ad alterazioni ematologiche di tipo emorragico con epistassi e petecchie, diatesi emorragica, sanguinamento emorragico. Gli esami clinici misero in evidenza il fatto che vi era un’alterazione del processo di aggregazione delle piastrine, per cui la coagulazione avveniva in modo ritardato (Assisi et al., 2010. E’ stato ipotizzato inoltre che anche l’Auricularia auricula-judae (Bull.) Quél. = Hirneola auricula-judae (Bull.) Berk. presenti gli stessi effetti sulla coagulazione; tuttavia non sussistono dati scientifici al riguardo (Assisi et al., 2010).
Principi attivi
I principi attivi ancora non sono stati isolati, secondo (Makheia & Bailey, 1981) entrerebbe in gioco l’adenosina, un inibitore competitivo dell’aggregazione piastrinica, avente effetti antitrombotici, presente nell’Auricularia polytrica, nella cipolla e nell’aglio. Ingerendo questo fungo verrebbero altresì ad aversi modifiche del AMP ciclico (Assisi et al., 2010). Secondo (Benjamin, 1995) le cause sono invece ancora da individuare. Nel caso dell’Auricularia polytricha contribuiscono alla sintomatologia clinica, pasti abbondanti e ripetuti nel tempo (Assisi et al., 2010). L’Aricularia polytricha è stata usata in passato per curare ipertensione, emorroidi, arteriosclerosi, traumi, patologie oculari, disturbi gastrici e dell’apparato genitale femminile (Gerard, 1633). La presenza di polisaccaridi contenuti nel fungo, vengono usati in micoterapia per stimolare il sistema immunitario, per la produzione di interferone ed interleuchine, le quali antagonizzano la proliferazione di cellule tumorali (Assisi et al., 2010). Inoltre alcune sostanze presenti nel fungo possiedono anche azione cardiovascolare, antivirale, antibatterica, antiparassitaria, riducendo anche il valore del colesterolo ematico. L’azione anticoagulante e fluidificante migliorerebbe altresì la vascolarizzazione sui vasi sanguigni, sulle stenosi, prevenendo in tal modo trombosi ed altre occlusioni vascolari, responsabili di infarti e di ictus (Assisi et al., 2010). L’Auricularia nigricans (Sw.) Birkebak, Looney & Sánchez-García = Auricularia polytricha (Mont.) Sacc., agisce sul collagene dei vasi, e verrebbe pertanto escluso il pericolo di emorragie interne (Assisi et al., 2010.
L’Auricularia polytrica è stata somministrata a topi in via sperimentale; dopo 4 settimane di trattamento, il gruppo trattato ha mostrato una significativa riduzione del colesterolo totale, mentre l’LDL e il colesterolo epatico non hanno presentato sufficienti riduzioni. Sono comunque stati dimostrati gli effetti dell’Auricularia polytrica sul colesterolo nei ratti, anche se però non si è riusciti ad evidenziare il meccanismo di azione (Assisi et al., 2010. Studi eseguiti su volontari (Chen Cheejen., 2004) hanno dimostrato che il fungo esplica un aiuto verso le manifestazioni di stipsi, cefalee, menopausa, gotta, diminuendo la viscosità ematica, i livelli di colesterolo, trigliceridi e glicemia. Estratti miceliari e di polisaccaridi extracellulari di Auricularia polytrica presentano inoltre azione inibitoria sulle cellule tumorali (Assisi et al., 2010). Per (Hammerschmidt D.E., 1980), l’assunzione abituale di Auricularia polytrica<, associata al consumo di porri e aglio, oltre a fattori genetici e ambientali, contribuisce ad una diminuzione in Cina di malattie aterosclerotiche (Follesa P. et al., 2009).
Sintomatologie cliniche
A distanza di circa 3 ore dalla ingestione del fungo, si evidenzia una disfunzione piastrinica, che persiste per 24 ore (Brunelli E, 2007). Altre disfunzioni presenti sono: alterazione dell’attività protrombinica, porpore emorragiche cutanee con emorragie sia interne che esterne, epistassi, petecchie, diatesi emorragiche, non riconducibili all’assunzione di antiaggreganti piastrinici.
Terapie
La Sindrome di Szechwan ha una incidenza bassa, si somministra la vitamina K soltanto se le emorragie sono abbondanti (Assisi et al., 2010]. La prognosi è benigna e la terapia è di tipo sintomatico. E’ utile per il medico attuare delle diagnosi differenzial) per differenziare altri tipi di porpore emorragiche.
(Testo da: https://www.micologiaprofessionale.it/sindrome-acromelalgica-o-eritromelalgica/)
Sindrome Morgana (Morganismo) da Clorophyllum molybdites
Il fungo implicato è il Chlorophyllum molybdites (G. Mey.) Massee, Bull. Misc. Inf., Kew: 136 (1898), una specie fungina presente in America, Africa, Madagascar, Oceania, isole del Pacifico. E’ stata rinvenuta in Sicilia nel 2005 (Signorino C., 2006) ed in Sardegna nel 2008 dal micologo Alberto Mua (Follesa P. et al., 2009). Il fungo somiglia molto alla Macrolepiota procera (Scop.) Singer, e specie simili. Sottoposto ad una cottura prolungata, 70 °C per 30’ non si hanno problemi di intossicazioni, (Migliozzi V., 1996) anche se non vengono eliminate le tossine (Assisi et al., 2010).
Tossine
E’ stata estratta una tossina, ancora da identificare, avente azione tossica su topi e pulcini, costituita da un residuo proteico ad alto peso molecolare, termolabile e in parte resistente alla degradazione proteolitica, la quale sarebbe legata alle cause delle intossicazioni (Assisi et al., 2010). Si ipotizza la presenza di ammine aromatiche corresponsabili nella tossicità. Per (Floch., 1996) la carne a contatto dell’aria, vira dal colore bruno al bruno verde, subendo un processo di detossificazione. Sia la somministrazione per via parenterale che sottocutanea sono dose dipendenti; invece non vengono registrati effetti tossici per via orale (Follesa P. et al., 2009).
Sintomatologia
Le tossine agiscono a livello intestinale. La sintomatologia clinica si ha dopo 30 minuti (2-4 ore) con: nausea, vomito, diarrea (anche sanguinolenta), cianosi labiale, linguale, ungueale (senza alterazioni cardiovascolari o di tipo respiratorio). Dopo 24 ore dall’inizio della reidratazione per via endovenosa, il recupero è totale, anche senza l’ausilio di una terapia specifica. La cianosi è stata osservata spesso in Australia (Assisi et al., 2010) (Floch. et al., 1996). Anche per questa sindrome esistono diverse risposte da parte degli intossicati, le quali sono legate alle idiosincrasie e alla loro tipologia costituzionale; ciò spiega le diverse risposte di tipo clinico da parte degli intossicati
Terapia
Si utilizza il carbone vegetale in polvere e la lavanda gastrica, attuando il reintegro dei sali minerali, in caso di disidratazione (Assisi et al., 2010).
Valutazioni micologiche
La valutazione di tipo micologico, può essere effettuata attuando il riconoscimento sporale, oltre che su materiale fresco, quando presente, anche su reperti biologici (Follesa P. et al., 2009).
Sindromi a breve latenza
Nelle intossicazioni a breve periodo di latenza i sintomi si manifestano dopo 3-4 ore dalla fine del pasto. Questo tipo di intossicazione si manifesta con minore gravità ma con più frequenza. L'avvelenamento presenta un'evoluzione del quadro clinico che si risolve quasi sempre con esito positivo. L'organismo infatti risponde subito all'ingestione delle micotossine con meccanismi di difesa, quali: diarrea, vomito. Le sindromi da intossicazione di questo gruppo sono caratterizzate da tossine termostabili, che irritano le mucose dello stomaco e dell'intestino provocando i sintomi già nominati, danni al sistema nervoso (mal di testa, sonnolenza, riduzione dei battiti cardiaci e della frequenza respiratoria, diminuzione della pressione arteriosa).
Sindrome muscarinica
L'avvelenamento, e la conseguente sindrome, è causato dall'azione di una micotossina denominata muscarina, contenuta in funghi appartenenti ai generi Clitocybe e Inocybe; il quadro clinico si caratterizza per una certa iperattività del sistema colinergico, da cui consegue un aumento di produzione da parte delle ghiandole salivari, lacrimali, sudoripare e bronchiali. Dopo 3-4 ore dalla fine del pasto, possono cominciare a comparire sintomi gastrointestinali, ma fortunatamente l'esito è, nella maggior parte dei casi, favorevole. Le specie fungine responsabili della comparsa di questa sindrome sono diffuse ampiamente in tutta Italia.
Sindrome panterinica
Gli effetti sono, nella maggior parte dei casi, a spese del sistema nervoso, sia centrale che periferico. Funghi responsabili di questo tipo di sindrome sono l'Amanita muscaria, il classico "fungo delle fiabe", e l'Amanita pantherina. Queste specie possiedono la capacità di provocare avvelenamenti, più o meno gravi, grazie al loro contenuto di micotossine come l'acido ibotenico, il muscimolo, la muscarina (rispetto alle specie del genere Amanita si trova maggiormente in specie come quelle dei generi Clitocybe e Inocybe). I sintomi in questione possono essere sbalzi di umore come l'alternanza di momenti di iperattività, di eccitazione e momenti di torpore e sonno profondo. Se l'ingerimento dei funghi si svolge in maniera continuativa e regolare, le capacità neuropsichiche vengono compromesse gravemente; in seguito giungono manifestazioni convulsive, coma e morte. Da sottolineare però il fatto che le concentrazioni di micotossine in specie come l'A. muscaria varino a seconda del luogo di crescita e di raccolta della specie. In Siberia e in India, ad esempio, la specie viene consumata per i suoi effetti allucinogeni; nel nord Italia, per uso alimentare.
Sindrome psilocibinica
Forse l'unico tipo di avvelenamento causato volontariamente (le intossicazioni involontarie sono molto rare). Il quadro clinico che spesso si presenta assomiglia molto a quello dell'intossicazione da alcool. Nella maggior parte delle volte, si hanno allucinazioni che interessano tutti i sensi (vista, udito, tatto, olfatto, gusto). Le tossine agiscono sul sistema nervoso e sono la psilocibina e la psilocina, contenute nella specie Psilocybe mexicana. Altri generi che contengono tossine affini sono Panaeolus, Gymnopilus, Stropharia. L'azione di queste neurotossine è molto simile a quella delle droghe più potenti come l'LSD (dietilamide dell'acido lisergico).
Le specie che inducono questo tipo di sindrome sono riconoscibili per la loro morfologia caratteristica (si pensi al Panaeolus sphinctrinus) ma anche per le loro proprietà organolettiche. Infatti, alcune specie hanno un sapore acre e sgradevole. Il genere Psilocybe è caratterizzato da un forte odore di farina, con un retrogusto leggero di odore di rapa. Il genere Stropharia, invece, presenta una mescolanza tra odore di rapa e di lievito. Sebbene la maggior parte dei funghi appartenenti a questi generi si trovino prevalentemente in America centrale e del sud, altre specie come quelle appartenenti al genere Gymnopilus, come il Gymnopilus spectabilis e il già menzionato P. sphinctrinus, che hanno effetti allucinogeni, crescono anche in Italia.
Il consumo di funghi allucinogeni risale fino ai tempi più antichi. Gli effetti psichici erano ben noti già alle popolazioni indigene del centro America, come Incas e Aztechi. L'uso di queste sostanze era principalmente fatto per scopi religiosi come cerimonie, riti propiziatori, per entrare in contatto con le divinità, dare coraggio e ardimento ai combattenti prima di intraprendere importanti battaglie. Si verificano alterazioni neuropsichiche gravi, in cui il soggetto è portato addirittura a manie suicide e omicide, ma l'esito degli avvelenamenti è solitamente favorevole.
Sindrome coprinica
Sindrome che si manifesta solo se, all'ingestione dei funghi, viene accompagnato anche un contemporaneo consumo di bevande alcoliche. Il consumo di specie come Coprinus atramentarius, Coprinus micaceus e Boletus luridus può causare avvelenamento, se avviene insieme al consumo di bevande alcoliche, altrimenti non compare alcun malessere o disturbo gastrointestinale. Il C. atramentarius contiene una sostanza chiamata coprina che a contatto con l'organismo si trasforma in un altro tipo di composto, capace di influire sui processi di metabolizzazione dell'alcol, con un conseguente accumulo di acetaldeide. Se si presentano casi di avvelenamento, la gravità di questo può dipendere dal grado di tolleranza dell'alcol. Di solito l'evoluzione della sindrome è favorevole, dal momento che ai primi disturbi ci si accorge del vero motivo di origine del malessere e viene quindi interrotta l'assunzione di alcol almeno per 4-5 giorni successivi all'ingestione.
Sindrome paxillica
Sindrome causata dall'ingestione del Paxillus involutus. La specie è ritenuta pericolosa se mangiata da cruda, ma non se cotta o essiccata. Recenti studi osservano una forte tossicità dopo ingestioni tra loro ravvicinate nel tempo, ma si sono verificati casi di intossicazione anche con ingestioni avvenute a distanza di anni, molto spesso per intolleranza da parte del soggetto. I sintomi legati a questo tipo di intossicazione possono variare da una semplice allergia fino allo shock anafilattico. Nelle forme più gravi, con periodi di latenza intorno alle 4-9 ore, il quadro clinico peggiora e si verificano forme di anemia, a causa della distruzione dei globuli rossi, insufficienza renale acuta, riduzione della diuresi e collasso cardiocircolatorio. La sindrome è da considerarsi raramente mortale, ma ci sono stati casi in cui si sono registrati decessi.
Sindrome gastrointestinale
È tra le sindromi più frequenti, nei casi registrati. Il motivo è dato dal fatto che numerose specie fungine contengono le stesse tossine capaci di irritare la mucosa dello stomaco e del tratto gastrointestinale. La sintomatologia che ne consegue è caratterizzata da mal di testa, vomito, nausea, diarrea, crampi. L'esito è quasi sempre favorevole, perché il soggetto ha il tempo di correlare tra loro l'ingestione dei funghi con la precoce comparsa di disturbi intestinali. Disturbi che possono quindi allarmarlo, facendolo ricorrere a interventi sanitari, e sintomi come diarrea e vomito, aiutano nel frattempo a eliminare residui di cibo, e in generale, veleno.
Ci sono casi in cui il quadro clinico può avere andamenti sfavorevoli, talmente sfavorevoli da far assomigliare l'intossicazione a quella falloidea. Questo perché i veleni contenuti nell'A. phalloides sono gli stessi (o simili) a quelli contenuti nelle specie che provocano la sindrome gastrointestinale. I casi che hanno prodotto decessi, comunque, si sono verificati in persone come bambini, anziani, adulti già malati per altre cause. La disidratazione, la perdita di liquidi e sali minerali può aggravare la situazione fisica del soggetto, complicando l'apparato cardiocitcolatorio e portarlo infine alla morte.
I funghi responsabili di questa sindrome sono: l'Entoloma sinuatum, l'Omphalotus olearius, il Tricholoma pardinum, il Boletus satanas, l'Hypholoma fasciculare, il Lactarius torminosus, la Ramaria formosa.
Viene vivamente consigliato di astenersi al consumo di alcune specie fungine come l'Armillaria mellea, il Boletus erythropus, il Boletus luridus e la Clitocybe nebularis, anche se molti appassionati considerano ancora queste specie "commestibili"
Esistono altri avvelenamenti o intossicazioni da particolari funghi, se interessati fate ricerche in merito, io ho cercato di dare il più ampio quadro clinico.